
Wer sich an die Chemie- und Physikstunden erinnert, dem werden Begriffe wie „Ionen“, „Atome“, „Elektronen“ und „Protonen“ einfallen. Auch wenn Sie sie die Definition nicht jeden Tag herbeten müssen, allgegenwärtig sind die Naturwissenschaften doch – das gilt auch in der Bodenbearbeitung. Wie nimmt die Pflanze ihre Nährstoffe überhaupt auf, wie kann ein Boden basisch oder sauer sein bzw. werden? All das ist erklärbar mit den oben genannten Begriffen.
Kleine Erinnerung an den Physikunterricht
Atome bestehen aus Atomkern und Atomhülle. Im Atomkern befinden sich Protonen (positiv geladene Teilchen) und Neutronen. In der den Kern umgebenden Atomhülle befinden sich die Elektronen (negativ geladene Teilchen). Ist die Anzahl der Protonen im Kern gleich der Anzahl der Elektronen in der Hülle, befindet sich das Atom im Gleichgewicht, in sich stabil.
- Gibt das Atom jedoch Elektronen ab, herrscht also ein Elektronenmangel, ist das Atom positiv geladen. Man spricht von einem Kation.
- Nimmt das Atom stattdessen Elektronen auf, herrscht also ein Elektronenüberschuss, ist das Atom negativ geladen. Man spricht von einem Anion.
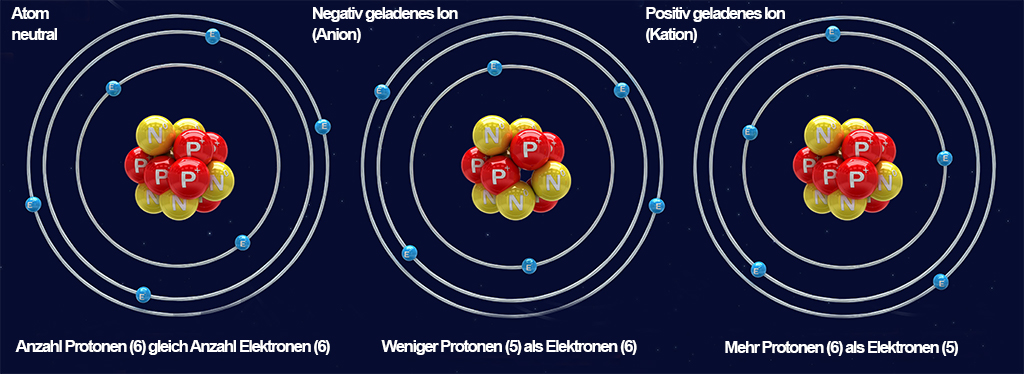
Kationen und Anionen sind Ionen. Die Begriffe leiten sich von ihrem Ziel (Pol) innerhalb eines elektrischen Feldes ab. Kationen drängen zur Kathode (Minuspol des Feldes) und Anionen zur Anode (Pluspol des Feldes).
Die Ionenbildung ist nicht auf Atome beschränkt. Auch Moleküle (Verbindungen aus mehreren Atomen) können Ionen ausbilden, das heißt, sie können negativ oder positiv geladen sein.
Der Begriff „Ion“ kommt übrigens aus dem Altgriechischen und bedeutet auf Deutsch „das Gehende“. Diese Metapher trifft es ganz gut: Ionen (also negativ oder positiv geladene Teilchen) wandern in einem elektrischen Feld von einer Seite zur anderen. All das geschieht hinsichtlich der Coulombkraft, der elektrostatischen Anziehungskraft. Plus und Minus ziehen sich an. Dieselbe Kraft sagt nun aber auch aus, dass sich Teilchen gleicher Ladung abstoßen: Plus und Plus, Minus und Minus stoßen sich ab. Dass der Atomkern, voll von Protonen, nicht auseinander bricht, dafür sorgen die Neutronen. Sie neutralisieren die Kräfte im Kern.
Unsere Nährstoffe sind Ionen
Wenn von Magnesium im Spargel die Rede ist, ist damit nicht gemeint, dass im Gemüse ein Stück Magnesium versteckt ist, sondern dass sich im Spargel Magnesium-Ionen (Mg2+) befinden, also geladene Teilchen vom Element Magnesium. Auch die Pflanze ernährt sich von Ionen. Idealerweise ist der Boden, auf dem sie wächst, voll davon.
Der Boden als Nährstoffspeicher
Fruchtbarer Boden besteht aus Ton und Ton wiederum aus negativ geladenen Ionen. Günstigerweise sind die meisten Nährstoffe positiv geladen. Das heißt Mg2+ ebenso wie zum Beispiel Ca2+ (Calcium-Ionen) können sich im Boden anreichern.
Welche Nährstoffe die Pflanze benötigt, um zu überleben, erfahren Sie im Beitrag Wovon ernähren sich Pflanzen.
Wasser als Medium
Im Boden als Produkt aus Anhäufung und Verwitterung sind die wichtigsten Nährstoffe (als Ionen) also vorhanden. Das heißt aber nicht, dass die Pflanze jeden Tag gleichsam darauf zugreifen kann. Denn damit die Ionen die Pflanze erreichen, braucht es ein Medium, einen Träger. Und das ist das Wasser (H2O), die wohl bekannteste Verbindung aus Sauerstoff und Wasserstoff.
Das Wasser hat die verschiedensten Aufgaben für die Pflanze. Eine davon ist der Nährstoff-Transport. Als Transportmittel wird es aus den Bodenporen (Zwischenräumen/Hohlräumen zwischen den Bodenteilchen) angesaugt. Dieser Sog entsteht, wenn die Pflanze selbst über weniger Wasser verfügt als der Boden um sie herum. Da die Pflanze permanent Wasser verliert (Transpiration), kann sie den Verlust durch das Ansaugen des Bodenwassers (Transpirationssog) ausgleichen und konsumiert die im Bodenwasser, der Bodenlösung, befindlichen Ionen (Nährstoffe). Im Boden werden Nährstoffe und Wasser von der Pflanze durch die Wurzel gewonnen, genauer: durch die Wurzelhaare.

Dass das Wasser als Medium genutzt werden kann, ist seiner Eigenschaft als Dipol zu verdanken. Das aus 2 Wasserstoffatomen und 1 Sauerstoffatom bestehende Molekül hat eine positive und eine negative Ladung. Das liegt an der Struktur des Wassermoleküls. Durch ein Elektronenpaar verbunden, liegen sich das eine Sauerstoffatom und die beiden Wasserstoffatome gegenüber. Das Sauerstoffatom kann dabei die stärkste Anziehungskraft auf die Elektronen ausüben und verschiebt somit den Schwerpunkt auf seiner Seite ins Negative. Es hat also eine starke Elektronegativität. Die beiden Wasserstoffatome, die sich in einem Winkel gegenüberliegen, haben eine geringere Anziehungskraft auf die Elektronen als das eine Sauerstoffatom, sodass auf ihrer Seite eher positive Ladung dominiert. Sie haben eine geringere Elektronegativität.
Aus diesem Grund ist das Wassermolekül sowohl positiv als auch negativ geladen. Es kann also sowohl negative als auch positive Teilchen an sich binden. Das ist der Grund, warum sich unser Speisesalz (Natriumchlorid; NaCl) in Wasser löst. NaCl besteht aus einem positiv geladenen Natrium-Ion (Na+) und einem negativ geladenen Chlorid-Ion (Cl–). Die Wassermoleküle brechen die Struktur auf, sodass sich nun beide Ionen voneinander gelöst im Wasser aufhalten. Dem Prinzip der Diffusion folgend, durchmischen sich die Teilchen und breiten sich aus. Auf diese Weise gelangen Wasser + Nährstoffe gemeinsam zur Wurzel. Innerhalb der Wurzel werden die Stoffe wieder voneinander getrennt. Während die winzigen Wassermoleküle passieren können, werden die Nährstoffe durch die halbdurchlässige (semipermeable) Membran daran gehindert. Das Passieren der Wassermoleküle durch die halbdurchlässige Membran nennt man Osmose.
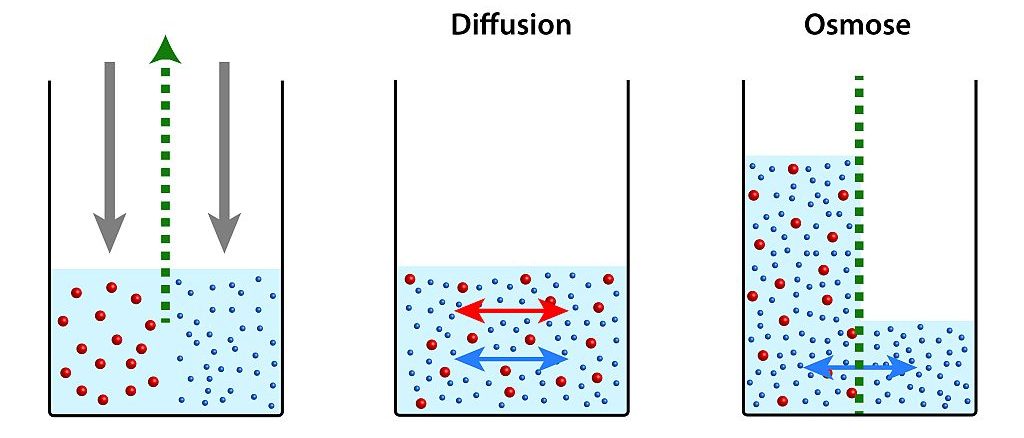
Solange genug Wasser (Bodenlösung) und gelöste Nährstoffe in der Lösung vorhanden sind, kann die Pflanze ihre Nährstoffe leicht konsumieren. Wird die Bodenlösung nährstoffärmer, werden bisher an die Bodenteilchen gebundene Nährstoffe per Ionenaustausch in die Bodenlösung abgegeben. Die Nährstoffe gelangen somit erst im zweiten Schritt zur Pflanze. Im Umkehrschluss bedeutet dies: Auch wenn der Boden noch so fruchtbar ist, ohne Bodenlösung wird die Pflanze die Nährstoffe schwer konsumieren können.
Ion gegen Ion – Ionenaustausch
Nach dem französischen Physiker Charles Augustin de Coulomb ist es so, dass bei Ionen mit gleicher Ladung (Plus oder Minus) höherwertige, stark bindende, Ionen die niederwertigen, schwach bindenden, Ionen verdrängen. Dieses Prinzip nennt man Ionenaustausch. Das positiv geladene Ion nimmt die Stelle des weniger bindungsfähigen positiv geladenen Ions ein. Die für die Pflanze wichtigsten Nährstoffe liegen als Kationen vor: Magnesium (Mg2+), Calcium (Ca2+) und Kalium (K+). Man spricht auch von Basenkationen. Über die Bodenlösung erhält die Pflanze ihre Nährstoffe. Man nennt Böden auch Kationenaustauscher, da Kationen gegen Kationen getauscht werden. Ebenso sind Böden Anionenaustauscher. Das Potenzial zum Haften und Austauschen von Anionen erhöht sich mit steigendem pH-Wert.
Als Abfallprodukt gibt die Pflanze Wasserstoff-Ionen (H+; auch Proton oder Hydrogen genannt) im Austausch für Kationen und u.a. Hydrogencarbonate (HCO3–) im Austausch für Anionen ab.
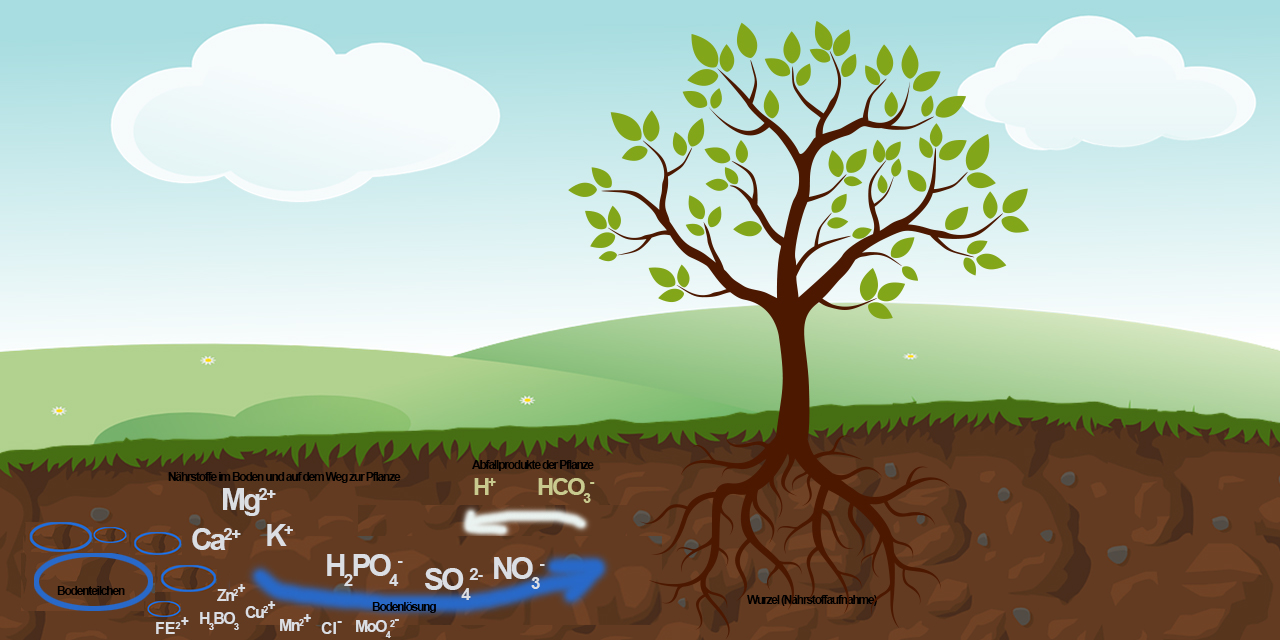
Die Fähigkeit des Bodens, Ionen zu binden und per Ionenaustausch abgeben zu können, ist überlebenswichtig für die Pflanze. Bekömmlich ist es jedoch nicht in jedem Fall. Bei gleichwertigen Ionen ist die molare Masse ausschlaggebend. So kann das „leichtere“ Kalium-Ion gegen das „schwerere“ Natrium-Ion ausgetauscht werden. Während Kalium für die Pflanze essentiell ist, spielt Natrium kaum eine Rolle. In ähnlicher Konkurrenz stehen auch die zahlreichen zweiwertigen Ionen (wie Magnesium, Calcium und Eisen). Zum Nährstoffmangel kann es daher auch kommen, wenn ein Nährstoff häufiger vorhanden ist als andere.
Widersacher Aluminium
Besonders fatal für die Pflanzenwelt ist die Dominanz von Aluminium. Dem Gesetz des Ionenaustausches folgend, kann das Al3+ (dreiwertiges Aluminium-Ion) praktisch alle zwei- und einwertigen Ionen und somit bedeutende Nährstoffe verdrängen und sich an ihre Stelle setzen. Aluminium-Ionen sorgen für Wurzelschäden und stören die Photosynthese. Bei einer günstigen Basensättigung sollten ca. 70 % der Basenkationen (Nährstoffe) im Boden vorhanden sein. Bei ungünstigen Verhältnissen könnten es ca. 30 % oder weniger sein. An ihre Stelle treten unter anderem H+ und Al3+.
Freie Aluminium-Ionen sind das Produkt einer Zersetzung von Tonteilchen, die u.a. aus Aluminiumsilikaten bestehen. Je saurer der Boden, also je mehr Protonen zum Austausch zur Verfügung stehen, umso höher ist der Zersetzungsgrad. Der Zerfall der Tonteilchen beginnt bei einem pH-Wert von ca. 4. Mehr über den pH-Wert in unserem Beitrag.
Saurer Regen ist aus eben diesem Grunde schädlich. Am Waldsterben ist dieses Phänomen gut zu erkennen. Die wichtigen Basenkationen werden durch Säurekationen wie Al3+ von oben nach unten ausgetauscht. Dadurch müssen die Pflanzen ihre Wurzeln tief nach unten wachsen lassen, um die Nährstoffe zu erreichen. Zuvor aber müssen sie die schädlichen und für sie giftigen Bodenschichten durchdringen, wobei sie die schädlichen Stoffe zwangsläufig in sich aufnehmen. Das nicht nur als Pflanzennährstoff, sondern für einen stabilen Boden wichtige Ca2+ (mehr im Beitrag Boden für die Pflanze) wird ausgewaschen. Der Boden verliert weiter an Struktur. Nährstoffe können nur noch bedingt im Boden gehalten werden und werden ausgewaschen.
Mehr über den Boden und dessen Beschaffenheit erfahren Sie im Beitrag Der Boden für die Pflanze.





Kommentar hinterlassen